Inhibition de l'oxydation des acides gras (FAO) abroge le cancer du sein triple négatif
Les preuves du rôle de la FAO excessive dans le cancer s'accumulent. Comme beaucoup de mes lecteurs le savent, le cancer du sein triple négatif est l'un des plus difficiles à traiter et sa proportion des cas totaux de cancer du sein a augmenté de manière constante au cours des 20 dernières années. Lorsqu'un patient est diagnostiqué avec ce type de cancer, les oncologues ne perdent pas de temps et mettent le patient sous un régime agressif de radiothérapie et de chimiothérapie cytotoxique, car ils pensent que c'est la seule chance du patient de survivre. Contrairement aux cancers plus courants sensibles aux hormones, les oncologues ne croient pas que ce type de cancer puisse être ralenti ou contrôlé au point que le patient vive avec lui comme une forme de maladie chronique sans qu'il ne devienne mortel. Sans dire, les thérapies métaboliques ne sont même pas mentionnées au patient simplement parce que l'oncologie ne croit pas que de telles thérapies aient une chance de traiter le cancer. Eh bien, l'étude ci-dessous est en désaccord. Elle met non seulement en évidence une fois de plus le rôle crucial de la FAO dans l'initiation/progression du cancer, mais elle démontre également que l'inhibition simple de la FAO peut arrêter complètement la croissance du cancer et assurer une survie de 100 % (voir Fig. 4e/4f ci-dessous). Le médicament FAO utilisé dans l'étude était l'étomoxir et c'est un inhibiteur de la CPT1 dit. La dose humaine efficace (HED) d'étomoxir qui a abrogé le cancer était d'environ 5 mg/kg par jour. Malheureusement, l'étomoxir est sévèrement hépatotoxique et, à ce titre, son utilisation clinique a été interrompue, il serait donc presque impossible de l'obtenir pour un usage humain ou de convaincre un médecin de le prescrire. Heureusement, le niacinamide est également un inhibiteur de la CPT1 et peut obtenir les mêmes effets que l'étomoxir avec une dose humaine d'environ 7 mg/kg. Sans dire, d'autres inhibiteurs de la FAO comme l'aspirine, le Mildronate/Meldonium, l'éthyl pyruvate + l'éthyl acétoacétate, la progestérone, etc. peuvent également être utilisés comme interventions et seront probablement très synergiques avec le niacinamide.
https://www.ncbi.nlm.nih.gov/pubmed/26950360
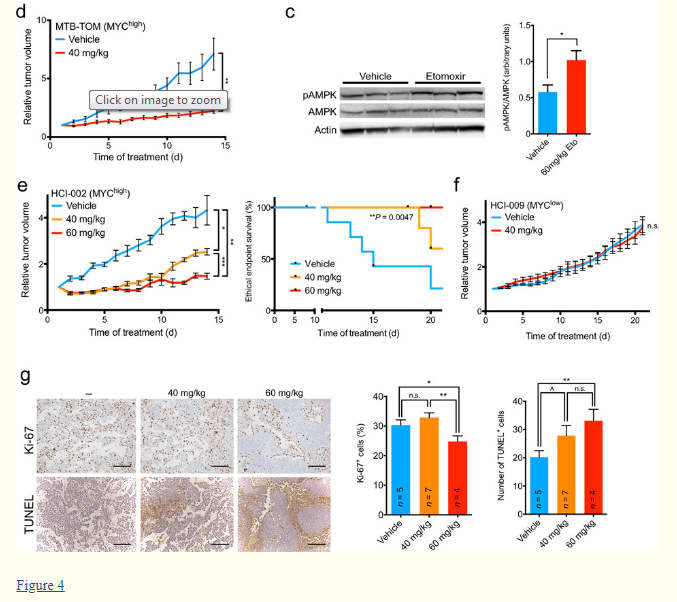
« …La réduction observée du métabolisme bioénergétique nous a amenés à analyser les effets de l'inhibition prolongée de la FAO sur la croissance des tumeurs MO-TNBC. Nous avons effectué un transfert orthotopique de tumeurs MTB-TOM ou HCI-002 PDX dans la glande mammaire de souris FVB/N ou NOD/SCID, respectivement. Nous avons administré 40 mg/kg d'étomoxir ou de véhicule par injection IP quotidiennement pendant 14 jours aux souris porteuses d'allogreffes MTB-TOM. Nous avons administré 40 ou 60 mg/kg d'étomoxir ou de véhicule par injection IP quotidiennement pendant 21 jours aux souris porteuses de tumeurs HCI-002 PDX. Le traitement par l'étomoxir a entraîné une atténuation significative de la croissance tumorale dans les deux modèles, et une extension significative du temps jusqu'au point de fin éthique dans le modèle PDX (Fig. 4d,e). En revanche, nous n'avons observé aucune atténuation significative de la croissance tumorale des tumeurs PDX TNBC HCI-009 MYClow traitées avec 40 mg/kg d'étomoxir (Fig. 4a,f).
« …Bien que le traitement par l'étomoxir de lignées cellulaires MO-TNBC en culture ait eu un effet marqué sur la prolifération cellulaire sans changements appréciables dans la mort cellulaire (Fig. 3 supplémentaire), l'inhibition de la FAO in vivo a entraîné une diminution concomitante de la prolifération et une augmentation de l'apoptose du MO-TNBC (Fig. 4g). Ces résultats sont cohérents avec le rôle plus critique de la FAO pour le développement tumoral in vivo. L'expression élevée de MYC a récemment été découverte comme un facteur définissant du TNBC1,2. La présente étude est parmi les premières à investiguer le rôle de MYC dans le métabolisme du TNBC in vivo. Ici, nous montrons que le MO-TNBC régule positivement la FAO, que le TNBC est sensible à l'inhibition de la FAO de manière dépendante de MYC, et que l'inhibition de la FAO abroge la croissance de modèles distincts de MO-TNBC in vitro et in vivo. Ce travail soutient un rôle critique pour la FAO dans le TNBC7,8, et identifie une dépendance à MYC comme marqueur de ce phénotype. L'inhibition de la FAO demande une investigation plus approfondie comme stratégie thérapeutique pour le MO-TNBC ».